ECMO(专题三)
22.11.10
ECMO在危重症新冠肺炎患者中的应用
孙兵 首都医科大学附属北京朝阳医院
卫健委医政医管局发布了《新型冠状病毒肺炎重症患者呼吸支持治疗和体外膜肺氧合临床应用指导方案(试行)》,推荐了新冠肺炎ECMO上机指征和相对禁忌证。上海、武汉、美国和法国新冠肺炎患者ECMO救治经验提示,患者启动ECMO的时机与既往差别不大。ELSO注册的国际队列研究显示,在779例ARDS患者中,657例患者有VV-ECMO前6 h内PaO2/FiO2记录,均值为72 mmHg(60~93 mmHg)。
ECMO支持时间长的可能原因:院内感染发生率高,MDR菌为主,抗感染药物种类多、级别高;支持中出现其他并发症;病毒转阴时间长,肺修复慢;ECMO管理团队的经验和团队人员配比。
目前并无证据显示新冠肺炎危重患者ECMO指征与以往有所不同,所谓更积极的治疗,仅仅是对我们应对不足、管理缺失进行弥补的权宜策略。
体外二氧化碳清除技术(ECCO2R)的临床应用
李绪言 首都医科大学附属北京朝阳医院
体外二氧化碳清除技术(ECCO2R)是由一个导管、一个泵、一个气体交换装置和一个控制器组成,临床曾试用血滤机器、血液灌流机连接膜肺实施ECCO2R。二氧化碳可以在较低的血流量下进行有效的清除。选择双腔13~15Fr导管,经股静脉或颈内静脉建立体外系统。影响ECCO2R疗效的因素:置管的管径,管路的再循环,人工泵的效能,膜肺的膜面积,心脏前负荷,低流量导致血栓形成,对膜肺性能的影响。
ECCO2R效能影响因素:膜面积固定后,ECCO2R效能取决于血流量和冲洗气流量,在膜两侧形成的氧气和二氧化碳压力梯度显著高于毛细血管/肺泡壁的压力梯度,达到清除二氧化碳的目的。血流量500~1000 ml/min时,冲洗气流量从1 L/min增加至14 L/min,二氧化碳清除非同步性提高,6~8 L/min基本达到平衡。酸化方法使血液中二氧化碳溶解度增加,提高二氧化碳分压,可提高清除效率,血流量可低至250 ml/min,置管管径可减少到13~15 Frs。
AECOPD患者ECCO2R治疗目标:患者舒适性好,pH>7.35/7.30(专家未取得一致意见);呼吸频率<20~25次/min,二氧化碳分压下降10%~20%,无创通气脱机,HCO3-下降,血流动力学稳定。
ECCO2R作为一种新型呼吸支持技术,日臻完善,既往在ARDS领域研究较多,但在AECOPD合并高碳酸血症呼吸衰竭患者中支持效果的评价近年来更受重视,期待更多临床研究证实。
ECMO出血并发症的防治
蔡书翰 武汉大学中南医院
ECMO患者出血并发症发生率高,严重出血直接影响患者结局。心脏术后和VA-ECMO出血和死亡率相对较高;ECMO患者置管部位和引流管出血最为常见,颅内出血致死率极高;ECMO患者可能发生出血部位多,应常规监测,及时探查。
病情危重、ECMO建立前抗凝APTT>70秒,外科术后ECMO患者出血风险高;心脏外科术后VA-ECMO中,pH<7.12、血红蛋白<9 g/dl、纤维蛋白原<2 g/L和BMI<25 kg/m2与早期主要出血事件显著相关;在VA-ECMO支持患者中,为了减少早期大出血,应采取早期积极主动的预防和治疗凝血病的策略。
心外科术后VA-ECMO出血风险更高;积极救治低血红蛋白和低凝血症应与ECMO运行的抗凝策略分开考虑;抗凝治疗需要常规监测出血情况;ECMO只支持期间尽量减少有创操作,尽早处理可见的出血。
危重症床边超声在ECMO支持中的应用
冯莹莹 中日友好医院
ECMO辅助前,超声可以进行患者评估和定位;ECMO建立时,超声能够引导穿刺;建立ECMO之后,超声可用于疗效评估。
(1)患者评估:①评价心血管情况及血管直径:选择合适的管路,判断有无变异或畸形等。②患者的选择:协助原发病的诊断。③评估既存的病生理状态:VA-ECMO的禁忌—主动脉夹层,主动脉瓣重度反流。
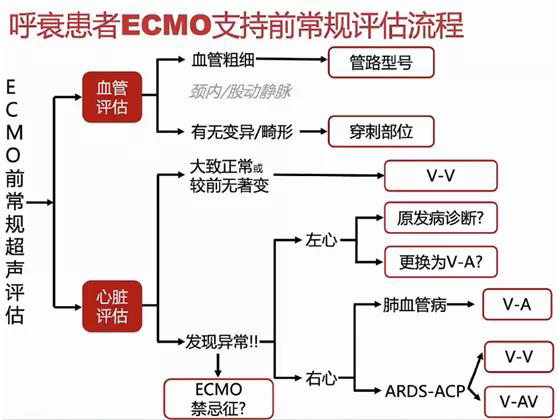
呼吸衰竭患者ECMO支持前常规评估流程如下图所示。

(2)ECMO建立时:通过二维血管超声,可以避免局部并发症,缩短穿刺时间,ECPR无法判断动静脉时。另外,可行超声引导下血管穿刺。J型导丝在超声下可清晰显影,确保进入目标血管,避免导致过深引起室性心律失常;确保扩皮效果和安全性,确认管路位置。
(3)ECMO建立后:反复通过心脏超声和血管超声确认管路位置;协助调整位置;发症的监测;指导治疗(VV-ECMO:难治性低氧;VA-ECMO:停搏的病因、肺水肿情况、撤机时机)。
ARDS的ECMO启动时机
罗红 中南大学湘雅二医院
ECMO主要是针对传统机械通气治疗无效的患者,解决患者低氧血症/高碳酸血症,降低死亡率,减少呼吸机相关性肺炎,但疗效仍存在争议。
2009年CESAR研究结果推荐潜在可逆的重症呼吸衰竭(Murray score>3分,pH<7.2)患者应用ECMO改善生存率,但其缺陷在于:ECMO组患者有5例在行ECMO前或转运途中死亡,传统对照组有部分患者后来为做了ECMO;缺乏标准的机械通气治疗,只有少数患者接受了肺保护性通气治疗。另有研究显示H1N1相关ARDS患者应用ECMO的死亡率显著低于未应用ECMO患者。2018年EOLIA研究提示ECMO组患者与对照组60天病死率无显著差异。一项系统回顾及Meta分析纳入了2项随机对照研究和3项观察性研究,结果提示ECMO治疗组患者30天和60天病死率均显著低于对照组。
清醒ECMO的优势:①无人工气道和正压通气能够避免呼吸机相关性肺炎和呼吸机诱导肺损伤的发生;②为维持患者清醒减少了镇静和镇痛药物的使用,利于早期活动和康复;③保留自主呼吸能够促进肺通气的均匀分布,减少呼吸机诱导膈肌功能障碍的发生。常用于等待肺移植的慢性终末期呼吸系统疾病和AECOPD患者。用于重度ARDS的经验较少。
ECMO是治疗中国ARDS的重要手段,在传统机械通治疗后,疗效仍不佳的患者可考虑启动ECMO;ECMO需要强大专业的团队实施。




